O GS1 DataMatrix é uma simbologia bidimensional, que permite codificar, com o uso de Identificadores
de Aplicação (AI), uma série de informações, como: identificação do produto (GTIN), data de validade,
lote, número serial etc.
O Art. 6º- da RDC 157/2017 determina que o DataMatrix codifique minimamente os seguintes dados que
compõem o IUM (Identificação Única do Medicamento), na seguinte ordem:
I – GTIN da apresentação;
II – Número de registro da apresentação do medicamento junto à Anvisa;
III – Código serial, de até 20 dígitos;
IV – Data de validade;
V – Lote de fabricação.
Com está norma, as empresas precisarão serializar os seus produtos. A serialização consiste em criar para cada unidade comercializável (SKU) dos produtos um número de série único.
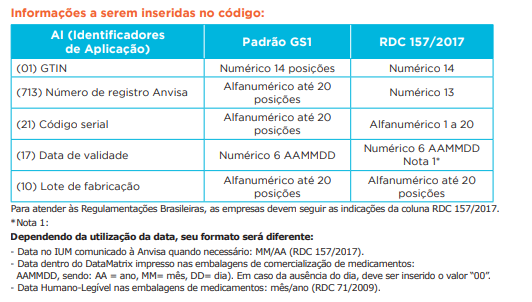
O número de posições mencionadas na RDC 157/2017 varia de acordo coma tabela abaixo:
Padrão GS1 RDC 157/2017
(01) GTIN Numérico 14 posições – Numérico 14
(713) Número de registro Anvisa – Numérico 13
(21) Código serial – Alfanumérico 1 a 20
(17) Data de validade – Numérico 6 AAMMDD *
(10) Lote de fabricação – Alfanumérico até 20 posições
DataMatrix Produto:
Sugestão de como codificar os requisitos da RDC 157/2017 (complementada pela RDC 319/2019) utilizando o GS1 DataMatrix:

É possível na parte Humano-Legível utilizar o AI (exemplo: (10)123ABC) ou especificar a informação (ex.: Lote: 123ABC).
Conforme regra de concatenação de dados e caracteres especiais para o exemplo acima, as informações ficariam organizadas da seguinte forma no GS1 DataMatrix:
010789835741001571332109876543212112345678901231718123110123ABC
<inicial>01078983574100157133210987654321<separador>211234567890123<separador>1718123110123ABC
Ex. de etiqueta logistica:

(00) SSCC – Código de Série de Unidade Logística: n2+n18
(01) GTIN – Número Global de Item Comercial: n2+n14
(17) USE BY/EXPIRY – Data de Durabilidade Máxima: n2+n6
(10) BATCH/LOT – Número de Batch ou Lote: n2+an20
*Dependendo da utilização da data, seu formato será diferente:
– Data no IUM comunicado à Anvisa quando necessário: MM/AA (RDC 157/2017).
– Data dentro do DataMatrix impresso nas embalagens de comercialização de medicamentos:
AAMMDD, sendo: AA = ano, MM= mês, DD= dia). Em caso da ausência do dia, deve ser inserido o valor “00”.
– Data Humano-Legível nas embalagens de medicamentos: mês/ano (RDC 71/2009).
Resumo da RDC 157 da Anvisa:
Docs adicionais:
